Дијагноза синдрома хроничног умора (МЕ/ЦФС)
May 19, 2022
Кључне речи:МЕ/ЦФС синдром хроничног умора; имунитет; дисбиосис;ЦОВИД-19; хормон; депресија; генетика; миРНА;терапија; дијагноза
1. Представљање
Мијалгични енцефаломијелитис/синдром хроничног умора (МЕ/ЦФС) је сложена хроничнаболест непознатог порекла која погађа скоро 0.9 процената популације широм света [1,2]. Симптоми болести су често широки и преклапају се са многим другим стањима, чинећиМЕ/ЦФС је тешко дијагностиковати. Претерани умор, малаксалост, бол у мишићима, неосвежавајући сан,Дисбиоза, когнитивна дисфункција и неуроендокрине и имунолошке промене су све пријављенекод пацијената са МЕ/ЦФС [3]. Док је МЕ/ЦФС често хронично стање, неки пацијенти могудоживљавају периоде делимичног опоравка између рецидива, а прогресија болести се разликујеуглавном између пацијената [4]. Иако се вирусне инфекције сматрају главним окидачемод почетка болести дуго времена, јасан механизам патогенезе је још увекнедефинисан [5]. Сада постаје јасно да би се порекло МЕ/ЦФС могло објаснити комплексомоднос између генетске предиспозиције и фактора животне средине, са сваком компонентомдоприноси манифестацији болести [6]. У том погледу, пол, социо-економски статус,и пријављено је да су у корелацији са појавом болести, при чему су женепретежно дијагностикована, али не нужно и чешће [7]. Иако је у литератури установљено неколико критеријума консензуса (тј. КанаДиан Цонсенсус Цритериа, Фукуда, Окфорд, Интернатионал Цритериа, итд.) без теста крви илидијагностички алат је комерцијално доступан [3]. Међутим, недостатак јединственог скупа дефинисанихкритеријуми консензуса могу довести до погрешне дијагнозе. Слично томе, и даље је јасан терапијски приступнедостаје. Иако су различите мета-анализе и клиничка испитивања показала снажне доказеу корист когнитивно-бихејвиоралне терапије (ЦБТ) и степеноване терапије вежбањем (ГЕТ) [8–17], треба спровести више истраживања како би се пронашли напредни терапијски приступи [6,18]. С обзиром на ова ограничења, идентификовање компоненти које доприносе болестипатогенеза и разумевање како они изазивају симптоме болести могу довести до новихдијагностички и терапијски приступи [6]. Неколико рецензија је доступно у литературибавећи се општим и специфичним темама у вези са МЕ/ЦФС, али потпуни прегледјош увек недостају различити аспекти који доводе до патогенезе и прогресије болести. Ину овом прегледу свеобухватно се бавимо дисфункцијом имунитета, хормонском неравнотежом,генетика/епигенетика и когнитивне промене утичу на пацијенте са МЕ/ЦФС, пружајући увиду појаву улоге некодирајућих РНК и промена цревног микробиома у болестипатогенеза. На крају, такође укључујемо кратак резиме потенцијалног односа измеђуновостворени „дуго-ЦОВИД“ и хронични умор.

Кликните овде да бисте сазнали више детаља о цистанцхе против умора
2. Методе
Прегледати улогу упале, имунитета, генетике, епигенетике, когнитивних симптома, дисбиозу, некодирајуће РНК и хормоне у МЕ/ЦФС, извршили смо исцрпнупретражи у ПубМед-у (Национална медицинска библиотека САД) базе података публикација. Следећекључне речи су коришћене саме или у комбинацији: "синдром хроничног умора", "мијалгични енцефаломијелитис", "МЕ/ЦФС", "упала", "когнитивни симптоми", "дисбиоза", "микробиом", "миРНА", "некодирајућа РНК", "ЦОВИД-19", "дуго-ЦОВИД", "умор", "терапија","дијагноза", "цитокин", "генетика", "полиморфизам", "епигенетика", "ХПА оса", "депресија", "пропустљивост црева" и "инфекција". Најновије публикације су биле префериране, али неу нашем скринингу је наметнут рок ограничења. Штавише, књиге, опште новине,и институционалне веб странице су прегледане ради могуће интеграције.
3. Резултати
3.1. Улога упале и имунитета у МЕ/ЦФС
Као и друга међућелијска комуникација, хомеостаза имуног система је нерегулисанау ЦФС [19]. То значи да ће пацијенти са МЕ/ЦФС доживети симптоме повезанена имунолошке промене као што је висока осетљивост на инфекције, посебно горњихреспираторни тракт, дуго време опоравка, хронично отечени и осетљиви лимфни чворови,и често осећам грозницу [3]. Још није јасно да ли је ЦФС инхерентно ниског степенаинфламаторна болест или да ли је праћена само системском упалом [5]. Тхеосновни узроци за сваки од симптома још нису у потпуности разјашњени, алиследећи параграф има за циљ сумирање тренутног стања знања у овој области.У погледу стања упале у телу могу се уочити вишеструке променеЦФС пацијенти у поређењу са здравим људима. Инфламаторни, ћелијски посредован имунодговор је активан чак и када су патогени одсутни. Ово може бити ненормална реакцијана уобичајене антигене који су безопасни [20]. Овај ћелијски посредован имуни одговор јегенерално карактерише смањена функција природних ћелија убица (НК), смањен одговород Т-ћелија до антигена [21,22], и постојаност аутореактивних ћелија [23–25]. Тхена активирано стање имуног система указује и повећање биомаркеранеоптерин, који ослобађају моноцити и макрофаги, и висока концентрација одреактанти акутне фазе [5,26]. Са поремећеном функцијом НК ћелија, способност организма даборба против инфекција се смањује. Што је функција ових ћелија теже поремећена, тогори симптоми МЕ/ЦФС од којих пацијент пати обично су, а пацијената је вишевероватно ће добити рекурентне инфекције због супресије имунитета [3,27]. Може се и посматрати експанзију ефекторских меморијских ћелија које показују одзив типа 2 којизначи да постоји хронична упала ниског степена. Фенотипска промена у Т-помоћним ћелијама одТх1- до Тх2-ћелије су већ откривене раних 1990-их [3,28–30]. Т-ћелије такође показујуповећана експресија ЦД26 на површини, дефектне функције регулаторних ћелија, брза исцрпљеност ипоремећен ћелијски метаболизам [5,19,28,31]. Контрадикторне студије су објављене нада ли пацијенти са ЦФС показују повећање или смањење Т-регулаторних ћелија [32,33]. у наставку, пацијенти са ЦФС показују постојаност аутореактивних ћелија које могу генерисати аутоантителатоком уобичајених инфекција, на пример, против ß2-адренергичких рецептора и М3 ацетилхолинарецептори [23,24]. Неутрофили и лимфоцити су склонији апоптози одкод здравих особа [34]. Налаз упале ниског степена је такође подржан од стране измењеног цитокинапрофила, пријављено је да су нивои про-, као и антиинфламаторних цитокина повишени уподгрупе пацијената [5,21]. Међутим, о томе су објављене контрадикторне студијетема у зависности од метода које су коришћене [21,35]. Нивои цитокина који су честопријављени као повећани су ИЛ-1 , ИЛ-1, ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-12 [5] и ИЛ-2 [26,36,37], онекоји изгледају смањени су ИЛ-8, ИЛ-13, ИЛ-15 и ИЛ-23 [5,38,39]. Штавише, ТНФ- и ИФН- нивои су повећани као и они НФ-κБ, регулисани фактор транскрипцијецитокинима као што је ТНФ- и ИЛ{0}} [5,27,37,40–42]. Као што је раније поменуто, у целинирезултати ових студија нису коначни, на пример за ИЛ-8 и ИЛ-13, повећани нивоитакође су пријављени [38]. Један од разлога зашто се ови резултати могу толико разликоватиизмеђу студија може бити утицај других фактора као што су сан, гојазност, исхрана,и сазнања о стању упале у телу. Временска тачка мерењатоком прогресије болести такође може играти улогу. Ако се уоче промене, њих је највишеизражен у прве три године болести. Ово је од клиничког значаја јер омогућаваразлику између раног и касног стадијума МЕ/ЦФС [43]. Поред укупног цитокинанивоа, мрежа интеракција цитокина такође изгледа одступа од норме [39]. A хронично висок ниво цитокина може ометати одговор на стрес на телесне проблеме иможе делимично да објасни хронични умор и симптоме сличне грипу у искуствима многих пацијената.Није јасно шта тачно узрокује појаву симптома у МЕ/ЦФС, али вирусноинфекције и стрес су разматрани као могуће порекло болести, док је андодатна генетска компонента је такође вероватно [3,44–46]. Инфективни патогени као што су вирусиможе бити изворни узрок упалног стања активацијом антивирусног имунитетареакције, које затим покрећу системску упалу [5,26,34,45]. Највише вирусне инфекцијеЕпстеин-Барр вирус (ЕБВ) који се широко пријављује у вези са ЦФС је значајан бројпацијената пријављују појаву симптома након заразе ЕБВ [47–49]. Међутим, требало би да будеnoted that an estimate of >90 посто одрасле популације генерално је позитивно на прошлостЕБВ инфекција, а већина не развија МЕ/ЦФС. Хумани херпесвирус 6 (ХХВ-6) ихумани парвовирус Б19 такође су пријављени као могући узроци ЦФС [50–54]. Тхевероватноћа да ће пацијенти развити ЦФС након тешких вирусних инфекција или других болести као што супошто је лајмска болест стално пријављивана као 5 до 10 процената [55]. Без обзира на којевирусна инфекција може изазвати МЕ/ЦФС, специфичне имунолошке промене које су ЦФС и вируснеинфекције које имају заједничко укључују измењене елементе антивирусног одговора, на пример, 2-5А синтетаза/рибонуклеаза Л (РНасе Л) антивирусни одбрамбени пут у моноцитима, који јепосредован интерлеукином [3,31,56], и повишени нивои цитокина. РНаза Л затим уништава ћелијумембране код пацијената са ЦФС, укључујући митохондријалне мембране што узрокује додатнеоксидативни стрес [57].
Код акутних болова у грлу, пацијенти су врло често присутниwith a viral reactivation, which may also be accompanied by tender, swollen lymph чворови [3]. Поред вирусних инфекција, још једно могуће објашњење за дисрегулацијуинфламаторна каскада је оштећење осе хипоталамус-хипофиза-надбубрежне жлезде (ХПА),пошто је у овом погледу пријављен системски хипокортизолизам познато је даутиче на имунолошку хомеостазу и покреће Тх2-ћелијски идентитет [28,58] (погледајте и ХПА осустав). Пацијенти који су примали когнитивно бихејвиоралну терапију (ЦБТ) показали су ниженивои кортизола након третмана у поређењу са нелеченим пацијентима [58]. Више студија је пријавило повишене нивое оксидативног стреса код ЦФСпацијенти [5,34,59]. Чини се да је антиоксидативни капацитет смањен у подгрупама пацијената, али чак и код пацијената са нормалним антиоксидативним капацитетом, повећање оксидативног стресасе посматра. Активност оксидативних и нитрозативних путева је појачана док се нивоиантиоксиданси као што је цинк и ензими као што је коензим К10 су смањени [5,21,60,61]. То може довести до прекомерног стварања слободних радикала, који се не могу елиминисати и хоћеоштећују ћелије циљањем на масне киселине и протеине [5,21]. Они се тада препознају каоабнормално од стране имунолошког система и може делимично довести до хроничног инфламаторног стања. АнИгМ посредован имуни одговор усмерен против епитопа модификованих О&НС у МЕ/ЦФСпримећено је [5,61]. У овом контексту, митохондријална дисфункција, која је билатакође приметио [5], такође може играти улогу јер је ова органела кључна за реактивни кисеоникрегулација врста (РОС). РОС-индуковано оштећење митохондрија и повишени проинфламаторницитокини, који су такође последица вирусне инфекције, могу да се активирајуНФ-кБ транскрипција.Пошто се чини да су инфламаторни сигнални путеви генерално поремећени, једанмогуће објашњење симптома болести може бити поремећена баријера црева [45]. Хипотеза о пропусним цревима је подржана налазом против којег се нивои ИгА код пацијената са ЦФС-омлипополисахариди (ЛПС) грам-негативних бактерија су повећани, што је праћеноповећаном транслокацијом ових бактерија [5] и чињеница да ЦФС и иритабилна цревасиндром (ИБС) се често јавља заједно [62]. Још једно могуће објашњење за изреченоимуни одговор може бити аутоимуност. Неколико фактора подржава ову идеју, као што је ависока преваленција код жена која је уобичајена код аутоимуних болести, повећање упочетно запаљење, и да се често јавља као коморбидитет других аутоимуних болестиболести [3,47,55,63,64]. Као што је горе поменуто, ЦФС се може јавити након инфекције ЕБВ,што је такође познат фактор ризика за развој аутоимуних болести [65,66]. Ако пацијентисе лече против аутоантитела, стање се побољшава [25,64]. Оно што снажно говорипротив идеје да је ЦФС аутоимуна болест, међутим, је недостатак оштећења ткива.Поред ових разлика у основном стању имуног система код пацијената са ЦФС упоређенокод здравих људи, пацијенти такође доживљавају малаксалост након напора(ПЕМ) [55,67,68]. Једно могуће објашњење за ово може бити израженији имуни одговор уМЕ/ЦФС пацијенти након вежбања него код здравих људи [69]. Након вежбања, физичкиали и ментално, симптоми се обично погоршавају у року од 24 х, међутим, постоји контрадикторностдоказ против имуног одговора који одступа од норме, вероватно због разликау дизајну студија [68]. Извештаји су направљени о повећању гена ТЛР-4 и ИЛ-10израз после вежбања [69]. Док је експресија гена била повећана, циркулацијаЧини се да су нивои цитокина као одговор на вежбање слични у ЦФС и контролним групамау неким студијама, али се јако разликују у другим [69,70]. При проучавању комплементаодговор на вежбу код пацијената са ЦФС, пронађени су неки докази за јачи одговорнего у контролама. Ово је од интереса јер може изазвати измењени одговор комплементаПЕМ [69]. Штавише, чини се да пацијенти пате од повећаног оксидативног стреса брже идуже после вежбања од здравих контролора, а њихов антиоксидативни одговор је одложен исмањен [46,59]. Ово се уклапа чак и са вишим нивоом оксидативног стреса код ових пацијенатабез вежбања и подржава хипотезу да су неки од симптома узрокованикварови у регулацији РОС. Даљи налази указују на смањење нивоа АТП-а,повећан лактат, хиперактивна РНКаза Л активирана ИФН-ом и хиперактивна НФ-κБ у односу наздраве контроле. Све у свему, докази сугеришу да је имуни одговор пацијената са ЦФСвежбање је израженије него код здравих људи [70].
3.2. Генетске и епигенетске промене
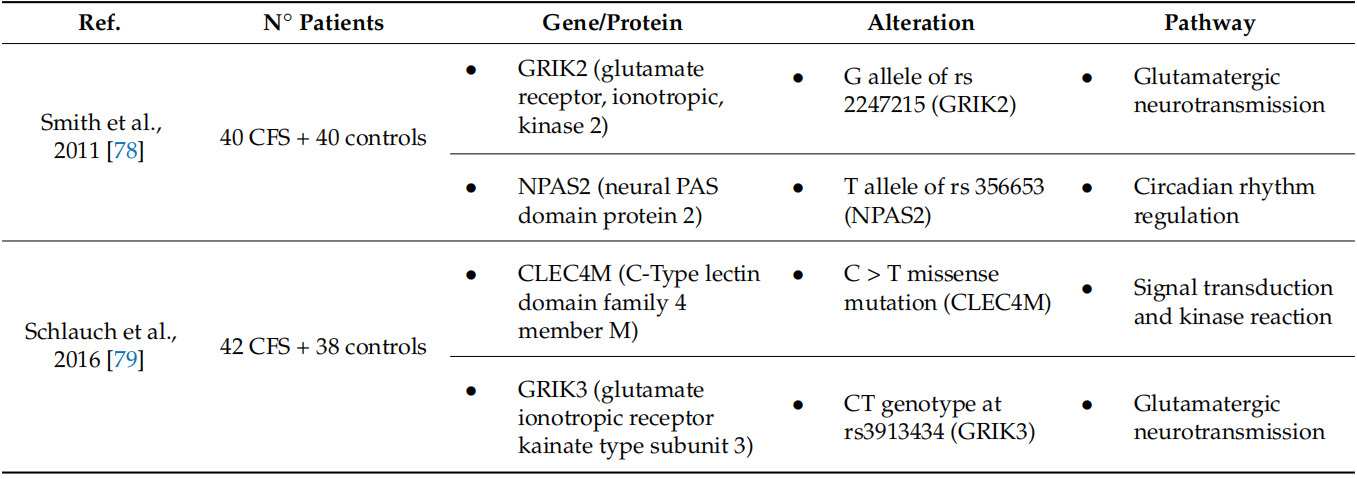
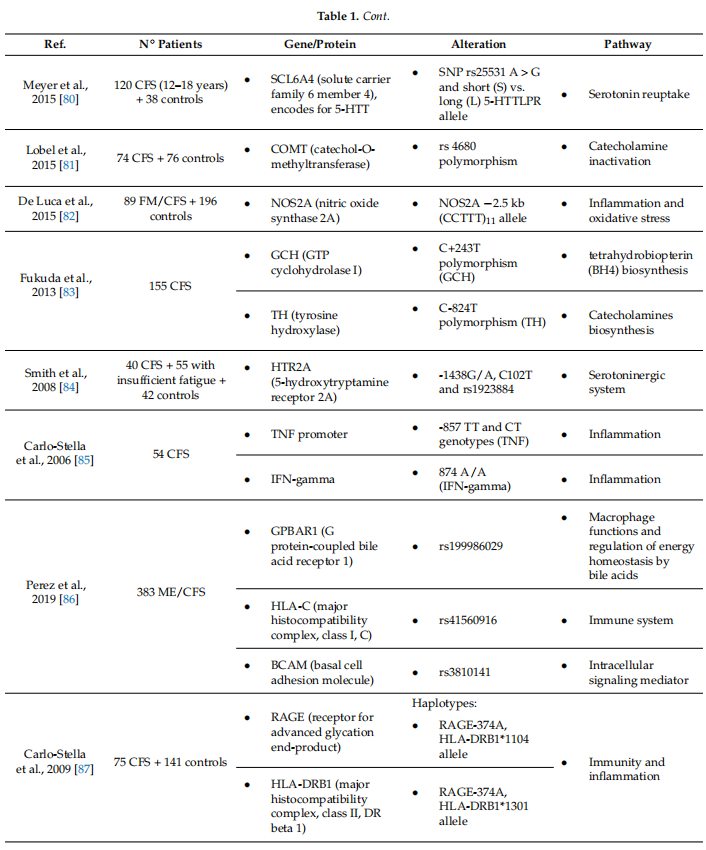
Иако је патогенеза ЦФС још увек у великој мери непозната, неколико студија указује на томогућност генетске предиспозиције. Први наговештаји дошли су из запажања да мајкеа деца са дијагнозом ЦФС имају веома сличне симптоме, за разлику од очева ињихова деца [71]. Штавише, анализа података добијених из здравствене заштите Јутесистем је истакао снажан допринос у корист ЦФС наследности [72]. Многи путевису затим повезани са симптомима и тежином болести, као што су регулаторни путевиимунитет и неуротрансмисија, запаљење и оксидативни стрес, катехоламинпут и серотонинергички систем [73] (Сто1). ТНФ- , ИЛ{0}} , ИЛ-4, ИЛ-6, ХЛА,ИФН- , ГРИК2, СЦЛ6А4, ЦОМТ и НР3Ц1 гени су сви у корелацијиса болешћу [73]. За резиме најзначајнијих налаза у вези са ЦФС игенетска предиспозиција погледајте табелу1. Упркос већини студија које извештавају о повезаности између ЦФС и једног или неколико полиморфизама, треба напоменути да, као мултифакторска болест, различит генетски доприносвећа је вероватноћа да ће објаснити предиспозицију и наследство него појединачна варијација. У овом погледу,многе варијације једва да доприносе саме по себи, али када се споје оне повећавајуризик. Стога ће потрага за хаплотиповима или комбинованим генетским полиморфизмима бити од помоћиу успостављању генетског скрининг теста који може да дијагностикује и/или стратификује пацијенте са ЦФС [74]. Можда би ово такође могло бити корисно за администрацију персонализованих и прилагођенихтерапија [75]. Такође се претпоставља да је генетска предиспозиција укључена у аутоимуност.Бломберг и др. представљају модел у којем се, након инфекције, одређују генетске позадинеа дисбиоза би могла да фаворизује стварање клонова Б-ћелија склоних да реагују на само-антигене,чиме се објашњава зашто неки пацијенти имају знаке аутоимуности [46]. Поред класичне генетике, све већи број доказа сугерише да епигенетикаје такође повезан са ЦФС и потенцијално може објаснити главне путеве укључене уболест. У једној студији, обрасци метилације 10 пацијената са ЦФС су упоређени са10 контрола, и имуни, метаболички и неуролошки путеви су повезани саболест [4]. Штавише, диференцијална метилација у гену ПРФ1 и у неколико ЦпГ локусаТ лимфоцита је такође откривена код пацијената са ЦФС за разлику од здравих субјеката [76,77]. Можда није изненађујуће, генетске и епигенетске промене које се налазе у ЦФС-у често постојеу истим генима и утичу на исте функције, чиме се потврђује значајпретходно поменути путеви у патофизиологији болести.Иако нова открића у ЦФС и генетици расту у очекивању у смислунових дијагностичких и терапијских средстава, треба сматрати да студије са вишпотребан је број учесника да би се постигао истински значај. Заиста, независноистраживања се обично спроводе на веома ограниченом броју случајева ЦФС и анализа наразличите групе пацијената често не успевају да репродукују одговарајуће резултате [74]. Стога, докнедавни подаци свакако могу повећати наше знање о механизмима болести и имапреводилачки потенцијал, потребно је више доказа који потврђују пре него што се ово знање примениу клиничкој пракси.

3.3. Когнитивни симптоми и депресија
Добро је познато да когнитивни симптоми као што су поремећаји спавања, депресија, анксиозност,а промене расположења се често налазе и карактеришу ЦФС. Заиста, недавна систематикапреглед и мета-анализа известили су да је око половина пацијената са МЕ/ЦФС присутнима саанксиозност и/или депресија [89]. Дијагноза ЦФС-а се постиже коришћењем добро утврђених дијагностичких критеријума (канадКритеријуми консензуса, Фукуда, Оксфорд, Међународни критеријуми итд.). У том погледу, пажљиводефинисање облика удруженог хроничног умора (тј. код рака, мултипле склерозе,инфламаторна болест црева и психијатријска стања) је критична за постизање закључкадијагноза. Типично, детаљна медицинска историја пацијента, укључујући симптоме,повезана инвалидност, избор стратегија суочавања и сопствено разумевање пацијентаузимају у обзир њихову болест. Пошто ЦФС и велика депресија (МД) деле веома сличнекарактеристике, многи пацијенти са ЦФС су у почетку дијагностиковани као депресивни [80]. иакодијагноза МД би требало да буде критеријум искључења за МЕ/ЦФС, правећи разлику између МДа реактивна депресија, која може бити коморбидитет ЦФС-а, није увек лака. Међутим,док ова два стања показују неке сличне симптоме, ипак се могу разликовати. Зана пример, код депресивних људи, умор је повезан са апатијом, док је код пацијената са ЦФСто је повезано са интензивном фрустрацијом због њиховог стања [90]. Поред тога, сваки ЦФСевалуација треба да укључи испитивање менталног статуса да би се идентификовале абнормалности у расположењу,интелектуалне функције, памћење и промене личности. Посебну пажњу треба посветитиусмерена ка акутним депресивним, анксиозним или самодеструктивним мислима и видљивазнаци као што су психомоторни проблеми. Штавише, физички преглед може показати ачесто бол у грлу и осетљиви цервикални или аксиларни лимфни чворови у ЦФС, који нисупронађен у депресији [90]. Као што је укратко поменуто, не само да постоји јасно преклапање симптома, већ и неколико чланакатакође показују да се МЕ/ЦФС и МД могу дефинисати као коморбидни [90]. Више разлога зао овој заједничкој појави се може расправљати. На пример, један од главних симптома ЦФС/МЕје хронични бол различитог квалитета и умор, а депресија је коморбидитет боласам [91]. Други могући разлог за овај коморбидитет може бити дисрегулација имуног система, као што је горе објашњено. Пацијенти са МЕ/ЦФС имају лоше функционисање НК ћелија,што је повезано са тежином болести и поремећеном когнитивном функцијом, док је нискаНК цитотоксичност је такође пронађена код других болести укључујући МД поремећај [3]. Скорашњирадови су такође открили да се током хроничне упале активирају микроглије иучествују у стварању неуро-инфламаторног окружења које се слично налази и код пацијенатаса депресијом [92]. Пропуштање црева и метаболичка ендотоксемија такође могу објаснити МД иПреклапање симптома ЦФС. Недавне студије су показале да се обе болести активирајуимуно-инфламаторни путеви, укључујући повећану транслокацију Грам-негативних бактеријаи виши нивои проинфламаторних цитокина, као што је ИЛ-1 [93]. Занимљиво, ухронична депресија повећани нивои ИЛ-1 повезани су са вишим нивоима умораи психосоматски симптоми, укључујући хипералгезију, несаницу и неурокогнитивнедефицити [94]. Штавише, депресија понекад такође произлази из ЦФС. Лоша концентрација, пипајући за речима, краткорочни губитак памћења и оштећење читањакод пацијената са ЦФС, са тешко погођеним пацијентима који доживљавају снажно онеспособљавање когнитивних функцијасимптоми [3,95]. Ово сложено психолошко стање често спречава пацијенте да наставењихов нормалан живот, што доводи до тешке депресије која заузврат може погоршати већозбиљни когнитивни симптоми.Међутим, немају сви пацијенти са ЦФС депресијом. Клинички извештаји пацијената са ЦФСбез историје депресије показују да третмани антидепресивима могу бити чак и штетниу овим случајевима [3,90]. Иако је клиничка дијагноза заснована на манифестацији симптомасвакако фундаментални, резултати неких студија сугеришу да се дијагностички алати на основумолекуларне и биолошке анализе могле би да побољшају дијагнозу. Док даља истрагапотребна је табела2 сумира предложене биомаркере на основу којих дијагностичких алатаможе се креирати да се направи разлика између ЦФС и МД (табела2). Треба напоменути да неуропсихолошки услови описани у МЕ/ЦФС имајупретпоставља се да потиче барем делимично од неуроинфламације. Виши нивоипроинфламаторни цитокини су пронађени у церебралној кичменој течности пацијената са ЦФС негокод здравих контрола, а активација микроглије и астроцита је верификована позитрономемисиона томографија (ПЕТ) скенирање. Прекомерна активност микроглије и астроцита показала је акорелација са озбиљношћу симптома код пацијената. Међутим, МД се не може приписатинеуроинфламација [96–98].


До данас не постоји стандардна терапија која би ефикасно ублажила симптомеболести. Међутим, постоје различити приступи који су испробанипрошлост која изгледа обећавајуће. Класични приступи су вежбање лечења полакоизградити повећану отпорност на умор и когнитивно бихејвиоралну терапију (ЦБТ) за ублажавањепсихолошки напор болести [3,55,58]. Главна забринутост код ЦФС-а је хроничнатретман бола.У том погледу, одговор на медитацију и опуштање, топле купке, масаже, истезање,акупунктура, хидротерапија, киропрактика, јога, Таи Цхи, ТЕНС (транскутана електричнанервна стимулација), физиотерапија и нервни блокови су сви предложени, али њиховаефикасност је још увек нејасна [3]. Иако су благи лекови против болова и нестероидни антиинфламаторнилекови (НСАИД), као што су ибупрофен и напроксен, могу се користити у клиничкој пракси запривремено ублажавају главобољу, бол у мишићима и грозницу, често не лече хронични бол,на тај начин не пружа олакшање на дужи рок [107–109]. Штавише, докази о њиховој ефикасностикао помоћна медицина у лечењу МЕ/ЦФС још увек недостаје [110], и нема великих клиничкихиспитивања подржавају њихов рецепт. Могуће објашњење за недостатак ефикасности у МЕ/ЦФСтреба тражити у пореклу бола код ових пацијената [111]. У том погледу, централносензибилизација, што је преосетљивост на бол због појачања неуронске сигнализације,може играти главну улогу. Нервни систем је подешен на високу реактивност на бол, што резултирахипералгезија. Неуролошке промене се могу приметити код ових пацијената, као што је ектопичнапуцање ћелија ганглија дорзалног корена или анатомске промене неурона и дорзалног рога.Неуроинфламација може можда допринети централној сензибилизацији. НСАИЛ могу и даљесе користе за модулацију активности ноцицептора, али антидепресиви су се показали вишеефикасност у управљању овом врстом бола док су физикална терапија и психотерапија такођекористан [112,113]. Често лекари саветују пацијентима са ЦФС да се физички одморе. Међутим, важно је да сеистичу да пацијенти, посебно они са депресивним поремећајем и без контраиндикацијаза физички стрес, требало би препоручити да се подвргне структурираном и надгледаном физичкомтренинг, јер се показало да терапија вежбањем побољшава симптоме код неких пацијената [114]. Подаци из осам рандомизованих клиничких испитивања су закључили да се физикална терапија побољшаваисцрпљеност, квалитет сна и здравствено стање пацијената на дужи рок, што се показујекористан потенцијал [12]. Овај налаз је у супротности са раширеним мишљењем да пацијентиувек се осећате непријатно након физичког напора, што је феномен познат као ПЕМ [115] Један од циљева лечења ЦФС је превенција депресије и суицидалних склоностиуправљањем физичким и емоционалним проблемима који произилазе из МЕ/ЦФС [3]. Краткорочнистудије ЦБТ у ЦФС су показале побољшање у функцији и управљању симптомима,посебно у комбинацији са другим модалитетима лечења и у поређењу са релаксацијомконтроле [116]. Симптоми умора снижавају расположење, а показује се и физичка спремностда се значајно побољша код пацијената након ЦБТ [9,11,14,15], чак и код децеи адолесценти [10,117,118]. Штавише, способност ЦБТ-а да ублажи бол у МЕ/ЦФС иматакође је пријављено [119]. Међутим, исход ЦБТ за ЦФС као психотерапеутинтервенција и ефикасност ЦБТ у побољшању когнитивних функција и квалитета живота и даљетреба у потпуности да се реши, пошто неке празнине остају у тренутној бази доказа [120–124]. С обзиром на преклапање са депресијом о којој је већ било речи, нијеизненађујуће је да би антидепресиви такође могли бити корисни у лечењу менталних аспеката ЦФС [124]. Велика мета-анализа укључујући 94 студије показала је да су антидепресиви приближно3,5 пута ефикаснији од плацеба у лечењу хроничног бола код пацијената са ЦФС [125]. Флуоксетин је, на пример, показао способност да побољша симптоме и имунолошку функцију [126] док се показало да је бупропион ефикасан у лечењу умора и депресијекод девет пацијената са ЦФС отпорним на флуоксетин [127]. Међутим, неки аутори подвлаче недостатакстудије о ефикасности антидепресива у лечењу МЕ/ЦФС и више студија о различитиммолекуле антидепресива треба спровести пре успостављања терапије [128].
3.4. ХПА осовина и хормонска неравнотежа
Када пате од МЕ/ЦФС, пацијенти могу доживети дисрегулацију у нивоимахормони које производи ХПА ос [129]. Заиста, упркос хетерогености симптомакоји утичу на пацијенте са ЦФС, и доказе мултифакторске патогенезе, хормонске неравнотежепоказало се да има директну везу са неким од симптома присутних уЦФС, као што су исцрпљујући умор, потешкоће са концентрацијом и поремећени сан [130]. У том погледу, докази мета-анализе подржавају присуство хипокортизолизма у ЦФСпацијената. Нивои кортизола су фундаментални за одржавање хормонске хомеостазе и кадаизмењени могу изазвати метаболичке, инфламаторне и меморијске промене, иако јестенисам сигуран да ли је запаљење узрок или последица хормонске неравнотеже. Штавише, агубитак јутарњег максимума АЦТХ (адренокортикотропног хормона) и смањена реакцијафармаколошки изазови су такође пријављени у случајевима ЦФС у поређењу са контролама [130]. Неколико симптома ЦФС-а личи на оне код хипотиреозе узроковане нижим хормоном штитне жлездеактивност која може бити последица основне хроничне упале. Студија контроле случајасу показали да пацијенти са синдромом хроничног умора показују нижи ФрееТ3 (тријодтиронин), ТТ3 (укупни тријодтиронин) и смањену периферну конверзију Т4 (тироксина) уТ3, нормалан/високо нормалан ниво ТТ4 (укупног тироксина) и ниже везивање штитне жлезде за протеинехормони [131]. Добро је познато да је преваленција ЦФС знатно већа код жена у поређењу са тиммушкарцима. Штавише, жене са ЦФС имају значајно већу вероватноћу да се пријаверанији почетак менопаузе због било каквих гинеколошких операција (хистеректомија иоофоректомија) као и бол у карлици и повезана ендометриоза у поређењу са контролном популацијом.Последице хистеректомије и раног почетка менопаузе ће довести до опадањау нивоу полних хормона. Низак ниво естрогена може утицати на имуни систем, узрокујућихронични умор и поремећаји спавања. Заиста, као деликатна равнотежа између естрогена ипрогестерон се губи, може настати неправилан одговор на упалу [132]. Сада је јасно да је правилна функција ХПА осе важна за хомеостазу. Каопацијената присутних са променама у ХПА оси, разумно је запитати се о могућимнеуроендокриних импликација у етиопатогенези ЦФС. Међутим, главно питање једа ли су промене ХПА умешане у генезу болести или су секундарнеразвоју ЦФС. У том погледу, ваљало би истражити која је улогаигра хормонска неравнотежа у патогенези болести [133]. Једна популарна хипотеза јетакозвано "алостатско стање оптерећења", где неуроендокрини систем реагује на астресор (алостатско стање) како би се ресетовала физиолошка задата тачка (хомеостаза). Ако је ово механизам откаже, долази до алостатског преоптерећења и начина на који се тело носи састресор продужава стрес и хроничност стања [134]. Могуће, ова ситуацијаможе доћи до дисфункције ХПА осе. Међутим, јасни докази у прилог томесугестија још увек недостаје, а потребно је спровести још студија да би се разумела улоганеуроендокринологије у патогенези ЦФС [135].
3.5. Дисбиоза и цревна пермеабилност
Неколико радова је указало на промену састава микробиома црева уЦФС пацијената и укљученост дисбиозе у патогенезу болестипретпостављено [136–138]. Конкретно, смањење микробне разноврсности и пад уБрој Фирмицутес је пронађен код пацијената са ЦФС у поређењу са контролном [137]. Штавише,друге студије су потврдиле смањење односа Бацтероидетес/Фирмицутес и повећањеЕнтеробацтериацеае, чиме се доказује потпуна реорганизација у цревимасастав и функција микробиома [139,140]. Употреба промене микробиоте као адијагностички биомаркер је такође предложен, али се болест преклапа са другим цревним поремећајимаможе представљати узнемирујући фактор током дијагнозе и стратификације пацијената [138]. Иако је микробиом црева кључан у различитим поремећајима, улога дисбиозе уПатогенеза ЦФС остаје да се у потпуности позабави, а њена улога у овој болести је још увек у порастурасправља [141]. Након секвенцирања 18С РНК у столици 49 пацијената са МЕ/ЦФС и39 здравих особа, Мандрано ет ал. пријавили незнатну разлику у еукариотскимразноликост [142]. Због тога је потребно више студија да би се у потпуности разумео микробиом цреваучешће у патогенези и прогресији болести.Дисбиоза је добро познати узрок повећане пропустљивости црева. Овај феномен,такође познат као црева која пропуштају, омогућава транслокацију бактерија у крвоток, чиме се повећавасистемско запаљење путем имунолошког одговора посредованог вишим нивоима ЛПСизведено из Ентеробацтериацеае [26,143–145]. Више комензалне бактеријске транслокацијеи повећана инфламација црева је пријављена у случајевима МЕ/ЦФС у поређењу саздраве контроле, слично ономе што је већ пронађено код гојазности, дијабетеса, метаболизмасиндром, неалкохолна масна болест јетре и септички шок. [143,145–148]. Терапеутскиинтервенције које имају за циљ поновно успостављање аеробиозе и смањење цревне пропустљивостиможе бити од помоћи у овом погледу. Показало се да исхрана са пропусним цревима, заједноса антиинфламаторним и антиоксидативним супстанцама, може значајно да се побољшаЦФСУслови [149]. Штавише, употреба пробиотика и/или пребиотика такође треба да будеразматрају, а прелиминарне студије на мишевима и пацовима показују обећавајуће резултате [150–153]. Коначно, пријављени су позитивни резултати коришћењем трансплантације фекалне микробиоте (ФМТ) уЦФС пацијенти [154], али су потребни додатни докази. Поред тога, неколико забринутости окоФМТ, на пример, недостатак доследности, проблеми са донаторима, дугорочна безбедност, итд., и даље се јављајусумње у сигурност и изводљивост, ограничавајући његову употребу у клиничкој пракси [155–159]. Све у свему, ови подаци указују на укљученост цревног микробиома у болестпатогенезу и прогресију треба даље анализирати, а тај обећавајући нови терапеутскиалати који циљају на црева која пропуштају и дисбиозу могу потенцијално да се појаве код пацијената са ЦФС.

3.6. Не-кодирајуће РНК
Некодирајуће РНК (нцРНА) контролишу различите нивое експресије гена, хроматинаархитектура, епигенетско памћење, транскрипција, спајање РНК, уређивање и превођење [160]. Једна специфична врста нцРНА, микроРНК (миРНА), мења и модулира неколико развојних, физиолошки и патофизиолошки процеси [161]. Ова модулација може битипостиже се на различите начине: утишавањем гена, покретањем цепања њихових одговарајућихциљне мРНК, или инхибицијом транслације гена након потпуног или делимичног везивања за њиховуциљна секвенца [162]. Измењена експресија протеина карактерише хронични бол и доприноси развојудуготрајне хиперексцитабилности ноцицептивних неурона на периферији. Штавише,централни нервни систем карактеришу експресионе промене сигналних молекула,трансмитери, јонски канали или структурни протеини [163]. Пошто су миРНА део механизамаекспресије гена, они ће вероватно допринети овим променама.Постоји потреба за непристрасним, специфичним дијагностичким биомаркерима за убрзање МЕ/ЦФСдијагноза и лечење пацијената, као што су неки претходно предложени биомаркери као што је активин Бо којима се контроверзно расправља [164,165]. миРНА профили представљају обећавајућу стратегију заоткрити биомаркере и у новије време да дијагностикује пацијенте. Ограничење за биомаркерстудије открића у МЕ/ЦФС је мали број учесника који су регрутовани.Пацијенти са МЕ/ЦФС показују диференцијалну експресију гена који кодирају миРНА који регулишуцитотоксичност, секреција цитокина и апоптоза [166]. Према томе, миРНА имају потенцијалда се користе као биомаркери за дијагнозу и прогнозу болести, али је императив пронаћиначин да се маркери учине што прецизнијим за пацијента, с обзиром на његов пол, године,и начин живота. Заиста, раније је показано да је диференцијална експресија миРНАу МЕ/ЦФС зависи и од пола, вежбања и стања болести. То је изузетно важнода усклади процену и извештавање са заједничким елементима података (ЦДЕ) код људиистраживање за побољшање квалитета података које омогућава поређења у више студија [167].
Путеви на којима свака миРНА испољава своју активност још нису јасни, али неколико миРНАидентификовани су као измењени код пацијената са МЕ/ЦФС.Већина миРНА различито експримираних код пацијената са ЦФС је укључена у имуни системрегулација одговора. На пример, повећана регулација миР-150-5п се види у обе Т-ћелијеи сазревање и диференцијација Б-ћелија и утиче на ослобађање проинфламаторног цитокинес. МиР-199-3п је негативан регулатор НФ-κБ и ИЛ-8. Ниски миР-199-3п израз,примећен код МЕ/ЦФС субјеката, повезан је са лошим исходом преживљавања код карцинома, што може утицати нафизиолошки терет повезан са болешћу. Још један нерегулисани миР-223 модулираТЛР4/ТЛР2/НФ-κБ/СТАТ3 сигнални пут последично утиче на инфламаторноекспресија цитокина [161]. Цитокини који се ослобађају као одговор на инфламаторни напад,посебно ТНФ- , директно потискују миР-130а-3п, смањујући упалу иповезани оксидативни стрес. МиР-146а регулише експресију СТАТ1 и смањује ИФН- секреције, што резултира губитком репресивног ефекта регулаторних Т лимфоцита, докмиР-374а-5п регулише експресију убиквитин лигазе, мТОР сигнални пут имоноцитни хемоатрактантни протеин (МЦП)-1, критичан за инфламаторни и имуни одговор.Прекомерно изражен миР-4443 повећава проинфламаторне цитокине активирањем НФ-κB путање преко циљања ТРАФ4. Израз миР-558, миР-146а, миР-150, миР-124,и миР-143 су директно повезани са већом експресијом имунолошких инфламаторних болестигени који кодирају ТНФ- , ИЛ-6 и ЦОКС-2 код адолесцената са ЦФС [161]. Поред тога, НКћелије су показале највеће промене у експресији миРНА са повећањем регулацијеод хса-миР-99б и хса-миР- 330-3п. Ово је у складу са МЕ/ЦФС фенотипомкарактерише променама активности НК ћелија [168]. Други важан фактор у МЕ/ЦФС је ендотелна функција. Тиха информацијарегулатор 1 (Сирт1) смањује упалу и оксидативни стрес и повећава производњуазотног оксида активирањем ендотелне синтазе азот оксида. МиР-21, миР-34а, миР-92а, миР-126 и миР-200ц регулишу функцију ендотела преко Сирт1/еНОС осе, али јенеопходно да се даље истражи како се ова регулатива дешава и њени извршиоци [169]. 2020. нова техника која се састоји од изазова стреса након напора који провоцираРазвијен је ПЕМ код пацијената са МЕ/ЦФС, што је омогућило да се добију мерења диференцијалаекспресија циркулишућих миРНА код тешко погођених пацијената. Ова студија је довела дооткривање и валидација једанаест миРНА повезаних са МЕ/ЦФС и стварањеалгоритам машинског учења који омогућава класификацију пацијената са МЕ/ЦФС у четирикластере повезане са озбиљношћу симптома, пружајући основу за развојновог неинвазивног теста за дијагнозу МЕ/ЦФС. Ови потписи и кластери миРНАпотенцијално се може користити за предвиђање одговора на фармаколошке третмане за МЕ/ЦФСи може чак омогућити клиничарима да идентификују појединце за које би такви третмани могли битиблаготворан [170]. МиРНА нису једини тип нцРНА са обећавајућом улогом у дијагнози ЦФС ипрогноза. Нове улоге дугих некодирајућих РНК (лнцРНА) у имунолошкој регулацији а откривају се процеси болести. Нивои у периферној крви мононуклеарнићелије (ПМБЦ) НТТ и ЕМКС2ОС (две лнцРНА повезане са имунолошким одговором)су повезани са тежим МЕ/ЦФС, што указује на потенцијалну дијагностичку вредностових лнцРНА. За НТТ је предложено да изврши своју функцију на оближњим генимаукључен у пролиферацију ћелија, апоптозу или упалу, због своје велике величине (17 кб). Апримећена је изражена позитивна корелација између НТТ и ИФНГР1, још једне лнцРНА, уМЕ / ЦФС, што сугерише да би НТТ / ИФНГР1 оса могла играти улогу у патогенези болести.Утврђено је да ниво експресије ЕМКС2ОС има повишене ПБМЦ код пацијената са ЦФС.Улога ЕМКС2ОС у ПБМЦ-у је тренутно нејасна и захтева више експерименатаразјашњено [171]. Заједно, претходно поменуте студије дају основу за развој интегралапрограм дијагнозе и прогнозе који не укључује само метаболичке аналите већ имолекуларне, као што су миРНА или лнцРНА, за дијагнозу и избор најбољег третманаза пацијенте са МЕ/ЦФС.
3.7. МЕ/ЦФС и ЦОВИД-19
Од августа 2021. године, епидемија корона вируса 2019. (ЦОВИД-19) узрокованаТешки акутни респираторни синдром корона вирус 2 (САРС-ЦоВ-2) довео је до скоро 216 милионакумулативних случајева, са 4,5 милиона смртних случајева широм света (СЗО, 2021, приступљено 31. августа 2021.).Клинички интерес је недавно прешао са акутне на хроничну фазу ЦОВИД-19што изазива додатне проблеме у управљању болестима. Заиста, део ЦОВИД-19преживели не успевају да се врате у своје претходно стање и пријаве упорне исцрпљујуће симптомеупоређено са ЦФС неколико месеци након акутне инфекције ЦОВИД-19резолуција [172–174]. Овај хронични поствирусни синдром назван је као „дуго-ЦОВИД” или „постакутни ЦОВИД-19 синдром" и пријављено је да утиче на пацијенте без обзира на тежину болестиакутна инфекција [175]. Међутим, треба напоменути да термин „дуго-ЦОВИД“, иакокоји се данас широко користи, још увек је слабо дефинисан, као и вишеструки ентитети изван хроничног умораукључени, чиме се постављају питања о коначности студија о дуготрајном ЦОВИД-у. Ину том погледу, основна истраживања о основним молекуларним и ћелијским механизмима могу бити одод велике помоћи у дефинисању више о односу симптома пост-ЦОВИД-19 и МЕ/ЦФС.Процене дуготрајног ЦОВИД-а увелико варирају у зависности од времена праћења. Једна студија извештавада је скоро 90 одсто од 143 пацијента искусило бар један симптом, посебно умори диспнеја, два месеца након опоравка од акутне инфекције [176]. Проценат пацијенатаса упорним симптомима након девет месеци праћења је пријављено да је пао на 30 процената,према лонгитудиналној проспективној кохортној студији која такође укључује амбулантне пацијенте са благимакутни ток болести, са умором, губитком мириса и укуса, и „можданом маглом“ међунајчешће упућене жалбе [177]. Са широким спектром симптома усредсређених на умор, маглу мозга, дифузну мијалгију,нересторативног сна и депресивних симптома, дуго-ЦОВИД подсећа на МЕ/ЦФС, што јечесто повезан са вирусним инфекцијама [178,179]. Занимљиво је да су кластери сличних МЕ/ЦФСсимптоми су примећени након других избијања коронавируса, укључујући САРС у2001. и МЕРС 2012. [180]. Смањен квалитет живота и упорни бол и уморпријављено 6 месеци након отпуста из болнице код 30 процената преживелих од САРС-а и МЕРС-а [181]. Осим тога, једна студија је известила да је 27 процената преживелих од САРС-а испунило критеријуме за МЕ/ЦФС41 месец након инфекције [182]. Штавише, у недавној мета-анализи пост-инфективнихсимптоми након САРС-а и МЕРС-а, умор је био најизраженији симптом у 19,3 одстопацијената до 39 месеци након разрешења инфекције [183]. Преваленција и трајање дуготрајних симптома ЦОВИД-а који личе на МЕ/ЦФС су и даљепод истрагом и постоје одређене несигурности због хетерогеног пацијентапопулације, трајање праћења и критеријуми укључивања [184]. Само неколико студија до садаприменили дијагностичке критеријуме за МЕ/ЦФС. Ретроспективна анализа је показала да 85,3 одстоод 231 преживелих од ЦОВИД-19 прикупљених из Геномске базе података летонске популације национална биобанка је достигла праг за дијагнозу МЕ/ЦФС, са три или више дугорочнихСимптоми слични МЕ/ЦФС који трају након 6 месеци [185]. Један центарпроспективна лонгитудинална студија открила је да само 13 процената од 130 пацијената са умереном до тешкомЦОВИД-19 пнеумонија је испунила критеријуме за МЕ/ЦФС 6 месеци након отпуштања [186]. У малој пилот студији у једном центру, карактеристике сличне МЕ/ЦФС пронађене су код 27 процената од 37 ЦОВИД-а19 преживелих, шест месеци након опоравка, без разлике у клиничкој инфламацији, плућафункција, лаки ланац неурофиламента серума (биомаркер оштећења аксона) и циљкогнитивно тестирање када се пореде пацијенти са карактеристикама сличним МЕ/ЦФС [187]. Друга студија је открила да је 14,2 одсто од 120 преживелих ЦОВИД-19 испунило дијагностику МЕ/ЦФСкритеријуми 6 месеци након појаве инфекције [188]. Серија случајева описала је обрасце сличне МЕ/ЦФСнакон решавања инфекције ЦОВИД-19 код три адолесцената и младих одраслих 6 месеци послеопоравак [189]. Упркос сличностима између симптома дуготрајних пацијената са КОВИД-ом и МЕ/ЦФС,потребни су додатни докази да би се ЦОВИД-19 уврстио међу инфекције повезане са МЕ/ЦФС.На крају, додатне истраге са дужим праћењем, јединственији критеријуми за МЕ/ЦФСдијагноза, укључујући и болничке и амбулантне пацијенте са инфекцијама различите тежине и аконтролну групу људи погођених другим инфекцијама потребно је да боље карактерише ризикфакторе, преваленцију и прогресију дуготрајних карактеристика сличних ЦОВИД МЕ/ЦФС, као и дизајнспецифичне интервенције и третмани.
4. Дискусија
Све у свему, представљени увиди показују да је МЕ/ЦФС сложена системска болестшто утиче на многе органе. Прегледом најважнијих путева и повезаних системаса патогенезом и симптомима болести, наш преглед подстиче да се узме у обзирМЕ/ЦФС као мултифакторска болест која се не може дијагностиковати или лечити на одговарајући начин ако јене разматра се у целини. Сходно томе, било која дијагностичка метода заснована на тестовима крвиили биомаркери треба да узму у обзир хетерогеност и сложеност болести. Штавише,интер-индивидуална варијабилност у манифестацијама МЕ/ЦФС је упадљива и треба је узети у обзиркада се развијају нова терапијска средства. Персонализовани и прилагођени приступи треба да будуупућују на терапију која одговара свима у овом погледу, али још много тога треба да се разјаснидефинисати специфичне подгрупе пацијената.Иако је хитно потребно више студија, наш резиме пружа општи прегледшто може бити корисно за боље разумевање МЕ/ЦФС патогенезе и проналажењенове дијагностичке/терапијске могућности за болест која, иако јако ослабљује,је још увек у великој мери неистражен.
ПРОНАЂИТЕ НАЈБОЉУ БОТАНИЧКУ ХОЛИСТИЧКУ НЕГУ ЗА СМАЊЕЊЕ УМОРА
Наша пажљиво ручно израђена формула Неуро Реген укључује најбоље истражено биље. Сваки од њих показује невероватан потенцијал за лечење против умора, плус општу подршку нерава и неурона.
Укључује:
① Цистанцхесадржи разне полифеноле и гликозиде, који могу повећати активност антиоксидативних ензима и имају функцију елиминације слободних радикала;
③ Цистанцхеима функцијуисхрана бубрега и јачање јанга,и може побољшати хипоталамус-хипофизу-хипофизу узроковану тешким вежбама. Функција осовине гонада подстиче лучење тестостерона, благотворно делује на анаболизам тела и делује против умора;
④ Цистанцхесадржи разне ефикасне састојке, који могу да подстичу енергетски метаболизам тела и играју улогуефекат против умора.