Први део МРИ са дифузијом у генитоуринарном систему
Jul 05, 2023
Апстрактан
Диффусион-веигхтед имагинг (ДВИ) представља главни функционални параметар који се изводи у снимању магнетне резонанце (МРИ). ДВ секвенца се изводи стицањем скупа природних слика описаних њиховим б-вредностима, при чему свака б-вредност представља јачину дифузионих МР градијената специфичних за ту секвенцу. Уклапањем података са моделима који описују кретање воде у ткиву, гради се мапа привидног коефицијента дифузије (АДЦ) која омогућава процену покретљивости воде унутар ткива. Висока целуларност тумора ограничава дифузију воде и смањује вредност АДЦ унутар тумора, што их чини хипоинтензивним на АДЦ мапама. Улога ове секвенце сада у великој мери превазилази њене прве клиничке појаве у неуроимаџингу, при чему је метода помогла у дијагностицирању раних фаза церебралног исхемијског можданог удара. Примене се проширују на снимање целог тела за неопластичне и не-неопластичне болести. Овај преглед наглашава интеграцију ДВИ у снимање генитоуринарног система тако што описује употребу секвенце у женској карлици, простати, мокраћној бешици, пенису, тестисима и МРИ бубрега. У гинеколошком снимању, ДВИ је суштинска секвенца за карактеризацију тумора грлића материце и карцинома ендометријума, као и за разликовање лејомиосаркома и бенигног лејомиома материце. Код епителних неоплазми јајника, ДВИ пружа кључне информације за карактеризацију чврстих компоненти у хетерогеним сложеним масама јајника. У снимању простате, ДВИ је постао суштински део мултипараметарског снимања магнетном резонанцом (мпМРИ) за откривање рака простате. Овом успеху значајно је допринео систем за извештавање и податке о слици простате (ПИ-РАДС) који мери вероватноћу значајних тумора простате. Његов допринос је успоставио мпМРИ као обавезни преглед за планирање биопсија простате и радикалне простатектомије. Пратећи сличан приступ, ДВИ је укључен у мултипараметарске протоколе за бешику и тестис. У имиџингу бубрега, ДВИ није у стању да јасно разликује малигне и бенигне туморе бубрега, али може бити од помоћи за карактеризацију подтипова тумора, укључујући карциноме бубрега са чистим ћелијама и карцинома које није са чистим ћелијама или ангиомиолипоме са ниским садржајем масти. Један од развоја бубрежног ДВИ који највише обећава је процена реналне фиброзе код пацијената са хроничном бубрежном болешћу (ЦКД). У закључку, ДВИ представља велики напредак у генитоуринарном имиџингу са централном улогом у алгоритмима одлучивања код рака карлице код жена и рака простате, сада омогућавајући обећавајуће примене у снимању бубрега или мпМРИ бешике и тестиса.
Кључне речи
генитоуринарни МРИ; дифузија; простате; бубрег; женска карлица; рак.

Кликните овде да бисте сазнали шта је Цистанцхе
Увод
У широком спектру клиничких метода снимања, дифузионо пондерисана МР слика (ДВИ) се истиче по својој изузетној вредности за управљање пацијентима, као и по својој фасцинантној техници. Са просторном резолуцијом близу 1 мм, секвенце пондерисане дифузијом (ДВ) испитују слободно кретање молекула воде у ткиву на нивоу микрометара, са фактором појачања близу хиљаду. Први пут уведен 1986. од стране Ле Бихана ет ал. [1], ДВИ је доживео велики развој након демонстрације своје способности да открије церебралну исхемију много пре било које друге неинвазивне методе [2,3]. Док је процес поремећене дифузије воде након ћелијског отицања још увек делимично схваћен [4], употреба ДВИ је брзо проширена на друге болести. Како се дифузија воде такође смањује у туморима због њихове велике ћелијске густине, многе успешне примене ДВИ су потврђене у онкологији и, иако су почетне примене биле ограничене на мозак, ДВИ се брзо проширио на друге делове тела укључујући генитоуринарни систем.
Генитоуринарни систем се обично истражује ултразвуком или аксијалном компјутеризованом томографијом (ЦТ) као модалитетима прве линије за откривање знакова малигних лезија или за стадијум болести. Ипак, магнетна резонанца (МРИ) се појавила као кључни играч у дијагнози и карактеризацији туморских и нетуморских болести, делом због свог супериорног контраста ткива. МРИ не само да даје морфолошке слике високе резолуције, већ пружа и различите функционалне информације, као што су оксигенација ткива, перфузија или дифузија. Међу овим функционалним техникама снимања, ДВИ свакако највише утиче на лечење пацијената са раком генитоуринарног система. Посебно, ДВИ је постао кључно средство у дијагнози и стадијуму многих гинеколошких карцинома и рака простате. Коначно, вођен напретком метода ублажавања респираторних покрета, ДВИ је такође успешно примењен на снимање бубрега.
Осим карцинома бубрега, ДВИ се појављује као алат у настајању који ће највероватније играти главну улогу у клиничком управљању нетуморним бубрежним болестима. Овај рад има за циљ да прегледа тренутне примене, као и потенцијалне будуће случајеве употребе ДВИ, са фокусом на женску карлицу, простату, бешику, пенис, тестисе и бубреге.

Цистанцхе тубулоса
Принципи дифузионо-пондерисане МРИ у генитоуринарном систему
Вода је најзаступљенији молекул у меким ткивима. Сваки молекул воде носи два нуклеарна окрета водоника, који су физички извор МРИ сигнала у огромној већини клиничких примена. Молекули воде пролазе кроз хаотично вечно микроскопско кретање, звано молекуларна дифузија, истражујући расположиве просторе у интра- и екстрацелуларним одељцима. У присуству јаког статичког магнетног поља, ови нуклеарни спинови водоника почињу да ротирају око осе поља у процесу који се назива прецесија. Фреквенција прецесије је директно пропорционална амплитуди статичког магнетног поља.
Добро позната техника спин ехо МР [5] даје интра-вокселно рефокусирање спинова „пресликавањем времена“ индивидуалних разлика у фреквенцијама прецесије. Ова померања фреквенције могу настати услед локалних нехомогености статичког магнетног поља или могу бити динамички индукована применом импулса магнетног градијента. Рефокусирање спин еха је несавршено ако се посматрани спинови подвргавају хаотичном кретању, што одговара делимичном губитку спин кохерентности и слабљењу интензитета спин ехо сигнала [6]. Дакле, посматрани МРИ сигнал садржи информације о молекуларном кретању воде и конкретно о ограничењу кретања услед различитих биолошких структура [4].
У слободном медијуму, вероватноћа да се лоцира дати молекул воде након датог периода је 3Д изотропна Гаусова функција, са пуном ширином на пола максимума (ФВХМ) која се повећава пропорционално квадратном корену времена посматрања. У овом случају, скаларна вредност, привидни коефицијент дифузије (АДЦ, мм2 ·с −1), одређује се као мерење величине дифузије [7], а слабљење МРИ сигнала је једна експоненцијална функција пондерирања градијента секвенце. Јачина таквих магнетних градијената је именована словом "б" иза којег следи нумеричка променљива која представља амплитуду и трајање примењених градијента, изражених у основним јединицама СИ од с·мм−2. Типични парови б-вредности варирају између 0–500 или 1000 с/мм2 за абдомен и 0–200 и 1000 с/мм2 за карлицу [8].
Код снимања простате вредности се крећу између 0 и 2000 с/мм2, на пример, б50, б500, б1000, б1500 и б2000. Дифузионо пондерисане секвенце које користе вредности градијента веће од 1000 с/мм2 могу се назвати ДВ секвенцама високих (или чак ултра-високих) б-вредности и њихов значај у МРИ простате је демонстриран у више студија [9,10]. У присуству таквих градијената, ако структуре сличне баријери ограничавају молекуларне покрете у ткиву, висок МР сигнал ће бити очуван и ткиво ће изгледати изразито хиперинтензивно на ДВ сликама и хипоинтензивно на АДЦ, што одражава смањену дифузију воде. У теорији, најједноставнији начин мерења АДЦ-а захтева само ДВИ аквизиције за две б-вредности и моноекспоненцијално уклапање, али су развијени и други сложенији модели како би се боље описали кретање молекула воде унутар биолошких ткива. Ови модели су углавном испитивани у простати и описани су у посебном одељку.
Пошто МРИ не узоркује директно објекат већ његове просторне фреквенције (депоноване у такозваном к-простору), он је посебно осетљив на кретање. Померање ткива током аквизиције доводи до умерених, а понекад и озбиљних артефаката [11], на пример, замућења, замагљивања и промене контраста ткива. Развијене су различите технике ублажавања да би се исправило кретање током аквизиције. Најосновнији метод за избегавање респираторног покрета је стицање слика током задржавања даха. Временска синхронизација аквизиције МР сигнала са физиолошким кретањем је затим добијена коришћењем окидања или синхронизације са ЕКГ или респираторним таласима. Сложенији приступи се састоје од праћења положаја ткива коришћењем навигатора заснованих на МР за проспективно или ретроспективно исправљање покрета. У клиничком окружењу, добијање висококвалитетних слика ДВ бубрега или карлице у оквиру једне апнеје није увек изводљиво. Због тога могу бити потребне технике компензације кретања да би се побољшао квалитет слике ДВИ и избегао збуњујући ефекат макроскопских покрета на дифузију воде [12,13].
Да би се додатно смањио ефекат физиолошког покрета, ДВИ се конвенционално добија коришћењем шема кодирања појединачних снимака које се називају ехо планарно снимање (ЕПИ). У ЕПИ, почетни РФ импулс побуде који генерише МР сигнал је праћен низом градијентних образаца и рефокусирајућих РФ импулса који покривају к-простор сваког пресека. К-простор у фреквенцијском домену се затим конвертује у слику помоћу математичке операције, Фуријеове трансформације. ЕПИ је склон геометријској дисторзији када је локално магнетно поље нехомогено и другим сложенијим артефактима, као што је несавршена засићеност сигнала масти. Једно решење за превазилажење ових ограничења је сегментација к-простора, али по цену повећаног времена аквизиције. Техника „Ресолве“ (РЕадоут Сегментатион Оф Лонг Вариабле Ецхо-траинс) [14] се састоји од скраћивања линија за очитавање у к-простору који су подељени на неколико паралелних опсега, најмање три. Ова функција омогућава смањење времена еха и времена кодирања фреквенције. Заузврат, техника даје оштрије слике које су генерално без изобличења и високе просторне резолуције, омогућавајући широку употребу код ДВИ простате и бубрега.

Цистанцхе цапсулес
Дифузијско пондерисано снимање женске карлице
Магнетна резонанца је комплементарни модалитет снимања који се обично изводи након ултразвука. ДВИ је кључан и изводи се у већини студија карлице код жена поред конвенционалних морфолошких Т1- и Т2-пондерисаних (Т2В) секвенци, као што је приказано на слици 1. ДВИ, заједно са динамичким контрастом побољшаним (ДЦЕ ) имиџинг, део је функционалног сликовног апарата који је у новије време повећао дијагностичке перформансе МРИ у области гинеколошке онкологије. Пошто ДВИ пати од лоше просторне резолуције, а самим тим и мање анатомске дефиниције, мора се користити заједно са морфолошком секвенцом Т2В [15]. ДВИ је посебно користан у процени карцинома ендометријума и грлића материце, помажући у разликовању бенигних и малигних лезија материце или јајника и процени ширења перитонеалног тумора код гинеколошких карцинома [16].

Слика 1. Нормална женска карлица 26-годишњака у короналној равни. (А) Т2В слика; (Б) АДЦ мапа; (Ц) б-вредност=0 с/мм2 ДВ слика; (Д) б-вредност=1000 с/мм2 ДВ слика. Видимо нестанак високог сигнала течности (као онај у бешици) са повећањем б-вредности, али постојаност високог интензитета сигнала на високој б-вредности за ендометријум.
Већина тумора грлића материце су карциноми сквамозних ћелија, за које се зна да су повезани са изложеношћу хуманом папилома вирусу (ХПВ) и чешћи од аденокарцинома грлића материце. Док је дијагноза доказана биопсијом, улога имиџинга у стадијуму рака је. Стадирање Међународне федерације за акушерство и гинекологију (ФИГО) је од суштинског значаја за онколошко терапијско управљање. Укључује карцином ин ситу (Тис), карцином ограничен на материцу (Т1), карцином који продире изван материце (Т2), карцином који се протеже до зида карлице и/или укључује доњу трећину вагине (Т3) и карцином који инвазира бешику или ректум (Т4). МРИ карлице се препоручује за локално одређивање стадијума тумора грлића материце као што је наглашено у ажурирању ФИГО стадијума из 2018. [17].

Екстракт Цистанцхе
Поред морфолошких Т2В секвенци, ДВИ се користи за процену локалног проширења карцинома и еквивалентан је МРИ са контрастом [18]. Аксијална коса раван Т2В окомита на дугу осу грлића материце је важна у процени параметарске инвазије (фаза ИИБ) и може се заједно регистровати са ДВ секвенцом високе б вредности да би се побољшало оцртавање туморског ткива [19], као што је приказано на слици. 2. Карциноме грлића материце карактерише хиперцелуларност која резултира високим интензитетом сигнала (СИ) на високој б-вредности (1000 с/мм2) ДВ сликама и ниским интензитетом сигнала (СИ) на АДЦ мапи у поређењу са нормалном стромом грлића материце [16]. До сада није потврђена гранична вредност АДЦ за предвиђање присуства малигнитета, углавном због међусобне зависности између израчунате вредности АДЦ и опсега б-вредности коришћених за прорачун [16]. У контексту праћења након локалне радиотерапије и системске хемотерапије, ДВИ се користи за разликовање резидуалне болести и локалне фиброзе [20], као и за откривање рецидива тумора [21]. ДВИ се такође може користити као биомаркер за праћење одговора тумора [22,23]. У недавној мета-анализи о употреби вештачке интелигенције (АИ) код гинеколошких тумора, рак грлића материце је био предмет великог броја студија (34 од 71) које су се углавном фокусирале на прогностичку вредност имиџинга [24]. Како се све МР секвенце користе колективно у АИ, остаје тешко екстраполирати специфичну корисност ДВИ унутар ове врсте приступа црне кутије.

Слика 2. МР слике 66-годишње жене са познатим карциномом грлића материце. (А) Сагитална Т2В слика; (Б) аксијална Т2В слика окомита на осу грлића материце. Рак грлића материце и његов продужетак који се појављују као нискоконтрастна Т2В област (стрелица) кроз нормалну строму и десни параметар, (Ц) висока б-вредност (б=1000 с/мм2) и (Д) фузионе слике између Т2В и секвенце високе б вредности за бољу процену проширења карцинома.
Карцином ендометријума је најчешћи гинеколошки малигнитет у развијеним земљама, који погађа жене старије од 50 година. Према Бокхмановом класификовању. (25), Тип И тумор ендометријума познат и као ендометриоидни карцином је најчешћи тип карцинома, са генерално повољним исходом. 2. по учесталости хистолошки тип карцинома ендометријума одговара папиларном јасноћелијском аденосквамозном карциному и припада група тумора типа лл. Према ФИГО класификацији, стадијум И тумора је ограничен на тело материце, а стадијум лл је дефинисан продужетком кроз цервикалну строму. У стадијуму ИИИ тумор локално инвазира на аднекс, вагина или параметар, и/или карлично дно, или представља пара-аорталну лимфаденопатију, док је стадијум ИВ дефинисан проширењем тумора на суседну бешику или црево или присуством удаљених метастаза.
МРИ код карцинома ендометријума се изводи ради стадијума болести. Инвазија мање од 50 процената миометријума за одвајање стадијума ла и Иб заснива се на морфолошкој равни Т2В која је окомита на ендометријалну шупљину. Рак ендометријума је обично хиперинтензиван за миометријум, али може бити тешко разликовати од околног ткива као што је илустровано на слици 3. На ДВИ рак показује ограничење дифузије са високим б-1000 сигналом и ниским вредностима АДЦ у поређењу са нормалним ендометријумом и суседни миометријум. Додатак ДВИ имиџингу Т2В значајно побољшава стадијум рака ендометријума (26,27). Још је незаменљивији код пацијената са оштећеном функцијом бубрега који не могу имати користи од примене гадолинијума, а самим тим и од МР-а са контрастом, међутим, комбинација ДВИ и МРИ са контрастом остају најбољи приступ за предвиђање инвазије миометријума, што је подржано недавном студијом о машинском учењу (28) ДВИ је такође од помоћи у откривању других таложења карлице у туморима високог степена (8). Лажно позитиван сигнал високог нивоа на ДВИ са ниским вредностима АДЦ у шупљини ендометријума одговара секреторном и хиперпластичном ендометријуму или крви током женског циклуса што се лако препознаје по високом сигналу на Т1В ФатСат секвенцама (8).

Слика 3. МР слике карцинома ендометријума код 93-годишње жене. (А) Сагитална Т2В слика у шупљини ендометријума са проширењем у миометријуму мањим од 50 процената његове дебљине. (Б) АДЦ мапа приказује ограничену дифузију у карциному ендометријума видљиву као тамно подручје (стрелица) у супротности са (Ц) високим сигналом (стрелица) на сликама високе б вредности (б=1000 с/мм?). (Д) Т1В слика након ињекције гадолинијума показује карцином ендометријума (стрелица) са повећањем мањим од мишића миометријума.
Леиомиосаркоми су ретки малигни тумори материце и чине мање од 10 процената карцинома материце. Разлика између бенигног леиомиома и леиомиосаркома је неопходна за хируршко лечење ових лезија. МРИ и посебно ДВл играју важну улогу у карактеризацији и управљању оба тумора. Поред морфолошких специфичности леиомиосаркома, као што су средњи Т2 сигнал, нодуларне ивице и хеморагијске компоненте, „Т2 тамне области и централне непобољшане области (параметри засновани на 291ДВ представљају још један суштински алат за разликовање бенигног лејомиома од леиомиосаркома 4. Као што је приказано на слици 4. , леиомиосарком материце обично показује ниске вредности АДЦ и повећан интензитет сигнала на сликама високе б вредности ДВ у поређењу са нормалним миометријумом (15). У мета-анализи Вираркара и сарадника која је укључивала 795 пацијената из осам студија, вредности АДЦ су биле значајно нижи код леиомиосаркома него код леиомиома (30). У недавној ретроспективној студији контроле случајева, Вахаб и сарадници су предложили дијагностички алгоритам за разликовање лејомиома од саркома материце на основу присуства лимфаденопатије са вишим СИ на сликама високе б-вредности у маси у односу на ендометријум и вредност АДЦ ниже од 0,905 к 10-3 мм?/с 31]. Одговарајућа осетљивост и специфичност овог алгоритма за класификацију маса материце била је 97 процената и 99 процената у сету за обуку од 156 пацијената, 88 процената и 100 процената у првом сету валидације од 42 пацијента, и 83 процената и 97 процената у другом сету валидације од 59 пацијената. Фокално или глобално редукована Т2В Сланд ДВИ базирана СИ нижа од ендометријума омогућава нам да са сигурношћу дијагностикујемо масу као бенигну [31]. Међутим, овај обећавајући приступ треба даљу валидацију проспективним мултицентричним студијама.
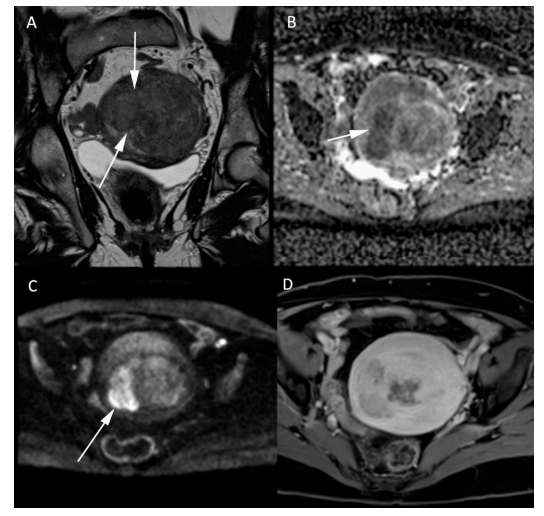
Слика 4. МР слике леиомиосаркома код 54-годишње жене. (А) волуминозни леиомиосарком са посредним сигналом од 2В и неправилним границама (стрелица). Део леиомиосаркома показује ограничење дифузије са ниским (Б) вредностима АДЦ и високим сигналом на (Ц) б-1000 секвенциД) после ињекције гадолинијума Т1 В секвенце показује одсуство централног појачања у складу са централном некрозом. Све карактеристике су карактеристичне за малигнитет унутар лејомиома.
Тумор јајника је углавном епителни тип рака (95 процената), укључујући серозни и муцинозни карцином. Две друге категорије укључују стромални тумор полне врпце и тип тумора заметних ћелија. Рак јајника је најсмртоноснији од свих гинеколошких карцинома, а прогноза је одређена почетним стадијумом у тренутку откривања. Прецизна карактеризација је, према томе, најважнија за пружање тачног одређивања прогнозе пацијента. Иницијална дијагноза се обично постиже ултразвучним прегледом, док се магнетна резонанца чува у неодређеним случајевима.
Нормални јајници обично показују висок СИ и на секвенцама високе б-вредности и на одговарајућим АДЦ мапама, што одговара такозваном ефекту "Т2 схине-тхроугх". ДВИ је неопходан за карактеризацију сумњиве чврсте компоненте у хетерогеним сложеним масама јајника, идентификујући чврсти садржај високе целуларности у малигним туморима јајника (32 према актуелним препорукама Европског удружења за урогениталну радиологију (ЕСУР) (33 Илустративне МР слике аденокарцинома могу се наћи у Слика 5. Корегистрација између ДВИ високе б вредности и морфолошких Т2В слика је веома ефикасна за ову сврху.Аднексална лезија се може класификовати као бенигна када је њена чврста компонента хипоинтензивна и на ДВИ високе б вредности и на Т2В снимцима (тамна/тамна" лезија) (34). Међутим, ДВИ сам по себи није довољан за процену малигнитета тумора јајника, јер неке бенигне лезије, као што су зрели цистични тератоми, ендометриоми или функционалне хеморагичне цисте, могу показати отежану дифузију ( 16, 32, 35]. Динамичке МРИ секвенце побољшане контрастом су неопходне за даљу процену вероватноће малигнитета.

Слика 5. Хистолошки доказан аденокарцином левог јајника код 64-годишње жене. (А) Т2Хиперинтензивна хетерогена лева аднексална маса поред материце (*). Ткивна дволупаста лева аднексална маса са деловима ниских (Б) вредности АДЦ и високог (Ц) б-1000 сигнала у складу са ограничењем дифузије у лезији (Ц). Након ињекције гадолинијума (Д) Т1В секвенца са засићеношћу масти показује хетерогено побољшање (стрелица).
Важна улога ДВИ-а у карактеризацији тумора јајника је добро демонстрирана у недавном увођењу система за оцењивање јајника-аднекса и система података (О-РАДС)-МРИ, међународног напора да се побољша стандардизација извештаја МРИ аднекса (36 ,37]. Т2В слике и ДВИ су довољни да се разликују лезије са чврстим садржајем у скоро сигурно бенигним случајевима (О-РАДС-МРИ 2) и вишим (О-РАДС-МРИ3 до 5), као образац побољшања хомогено хипоинтензивних лезија на Т2В и ДВимагес не утичу на О-РАДС-МРИ класификацију (37). О-РАДС-МРИ скор ризика је изграђен на основу проспективне, мултицентричне студије на 1194 жене са хистолошким прегледом и {{20} }годишње накнадно снимање или клинички преглед. Оцена ризика даје укупну тачност од 92 процента, осетљивост од 93 процента, специфичност од 91 проценат, позитивну предиктивну вредност од 71 проценат и негативну предиктивну вредност од 98 процената са добар договор између млађих и искусних читалаца, што потврђује капа-скор од 0,784 [36]. О-РАДС-МРИ валидација и клиничко прихватање су добро узнапредовали [38,39] и биће додатно побољшани када буду доступне препоруке за посвећено управљање [40].

Цистанцхе додатак
Морају се избећи неке замке у процени дифузионо пондерисаних слика. Као што је раније поменуто, Т2 просијавање, посматрано као упорни хиперинтензитет на сликама високе б вредности и АДЦ, један је од њих. Нису све структуре са високим сигналом на дифузију рак и треба бити свестан да здрава ткива могу дати ниске вредности АДЦ и висок сигнал на сликама високе б вредности: нормалан ендометријум, црева, бубрези, слезина и лимфни чворови [41,42] . Други критеријуми, као што су величина, хетерогеност и веома ниске вредности АДЦ, могу помоћи да се сумњиви лимфни чворови разликују од нормалних. Нормалан ендометријум код жена у репродуктивном добу такође може показати ограничену дифузију због велике густине ћелија ткива. У овом случају, мора се тражити квантитативна процена ткива на АДЦ картама, јер тумори ендометријума имају чак ниже вредности АДЦ у поређењу са нормалним суседним ткивом [15,16].
У закључку, ДВИ је кључан за одређивање малигнитета карличних лезија и за процену њиховог проширења. То је важан низ који мора бити део свих МР прегледа карлице. Анализа ових секвенци мора да користи и секвенце б-вредности и АДЦ мапу да би се избегла погрешна интерпретација и мора се упоредити са сигналом нормалне суседне структуре у карлици. Мора се анализирати у комбинацији са морфолошким секвенцама заснованим на Т2В, Т1В и гадолинијуму да би се избегла погрешна дијагноза неких бенигних карличних лезија као малигних.
Референце
1. Ле Бихан, Д.; Бретон, Е.; Лаллеманд, Д.; Грениер, П.; Цабанис, Е.; Лавал-Јеантет, М. МР снимање интравокселних некохерентних покрета: примена на дифузију и перфузију код неуролошких поремећаја. Радиологија 1986, 161, 401–407. [ЦроссРеф] [ПубМед]
2. Моселеи, МЕ; Цохен, И.; Минторовитцх, Ј.; Цхилеуитт, Л.; Схимизу, Х.; Куцхарцзик, Ј.; Вендланд, МФ; Веинстеин, ПР Рано откривање регионалне церебралне исхемије код мачака: Поређење дифузионо и Т2-пондерисане МРИ и спектроскопије. Магн. Ресон. Мед. 1990, 14, 330–346. [ЦроссРеф] [ПубМед]
3. Варацх, С.; Цхиен, Д.; Ли, В.; Росентхал, М.; Еделман, РР Брза магнетна резонанца дифузно-пондерисана слика акутног људског можданог удара. Неурологи 1992, 42, 1717. [ЦроссРеф] [ПубМед]
4. Ле Бихан, Д.; Иима, М. Дифузиона магнетна резонанца: Шта нам вода говори о биолошким ткивима. ПЛоС Биол. 2015, 13, е1002203.
5. Јунг, БА; Веигел, М. Спин ехо магнетна резонанца. Ј. Магн. Ресон. Имагинг 2013, 37, 805–817. [ЦроссРеф]
6. Стејскал, ЕО; Таннер, ЈЕ Мерења спин дифузије: Спин одјеци у присуству временски зависног градијента поља. Ј. Цхем. Пхис. 1965, 42, 288–292. [ЦроссРеф]
7. Сзафер, А.; Зхонг, Ј.; Андерсон, АВ; Горе, ЈЦ Дифузијско-пондерисано снимање у ткивима: Теоријски модели. НМР Биомед. 1995, 8, 289–296. [ЦроссРеф]
8. Европско друштво за урогениталну радиологију. ЕСУР брзи водич за снимање женске карлице. Смернице ЕСУР-а. 2019. Доступно на мрежи: хттпс://ввв.есур.орг/есур-гуиделинес/ (приступљено 1. марта 2022).
9. Катахира, К.; Такахара, Т.; Квее, ТЦ; Ода, С.; Сузуки, И.; Морисхита, С.; Китани, К.; Хамада, И.; Китаока, М.; Иамасхита, И. Ултрахигх-б-валуе диффусион-веигхтед МР имагинг за детекцију рака простате: Евалуација у 201 случају са хистопатолошком корелацијом. ЕУР. Радиол. 2011, 21, 188–196. [ЦроссРеф]
10. Охгииа, И.; Суиама, Ј.; Сеино, Н.; Хасхизуме, Т.; Кавахара, М.; Саи, С.; Саики, М.; Мунецхика, Ј.; Хиросе, М.; Гокан, Т. Дијагностичка прецизност ултра-високе б-вредности 3.0-Т дифузно-пондерисана МР слика за детекцију рака простате. Цлин. Имагинг 2012, 36, 526–531. [ЦроссРеф]
11. Заитсев, М.; МацЛарен, Ј.; Хербст, М. Артефакти покрета у МРИ: сложен проблем са многим делимичним решењима. Ј. Магн. Ресон. Имагинг 2015, 42, 887–901. [ЦроссРеф]
12. Цларк, ЦА; Баркер, ГЈ; Тофтс, ПС Побољшано смањење артефаката покрета у дифузионој слици коришћењем одјека навигатора и компензације брзине. Ј. Магн. Ресон. 2000, 142, 358–363. [ЦроссРеф] [ПубМед]
13. Пеи, И.; Ксие, С.; Ли, В.; Пенг, Кс.; Кин, К.; Ие, К.; Ли, М.; Ху, Ј.; Хоу, Ј.; Ли, Г.; ет ал. Евалуација симултаног вишеслојног дифузионог снимања јетре на 3.0 Т са различитим шемама дисања. Абдом. Радиол. 2020, 45, 3716–3729. [ЦроссРеф] [ПубМед]
14. Туллос, Х.; Дале, Б.; Бидвелл, Г.; Перкинс, Е.; Рауцхер, Д.; Кхан, М.; Џејмс, Ј. СУ-ЕИ-67: РЕСОЛВЕ више снимака у поређењу са шемом аквизиције МР слике са дифузно-пондерисаним ЕПИ једним снимком. Мед. Пхис. 2012, 39, 3640. [ЦроссРеф] [ПубМед]
15. Тамаи, К.; Коиама, Т.; Сага, Т.; Морисава, Н.; Фујимото, К.; Миками, И.; Тогасхи, К. Корисност дифузионо пондерисаног МР снимања за разликовање саркома материце од бенигних леиомиома. ЕУР. Радиол. 2007, 18, 723–730. [ЦроссРеф]
16. Вхиттакер, ЦС; Цоади, А.; Цулвер, Л.; Рустин, Г.; Падвицк, М.; Падхани, АР дифузионо пондерисано МР снимање тумора карлице код жена: сликовит преглед. Радиографија 2009, 29, 759–774. [ЦроссРеф]
17. Манганаро, Л.; Лакхман, И.; Бхарвани, Н.; Гуи, Б.; Гигли, С.; Винци, В.; Риззо, С.; Кидо, А.; Цунха, ТМ; Сала, Е.; ет ал. Стадирање, рецидив и праћење рака грлића материце коришћењем МРИ: Ажуриране смернице Европског друштва за урогениталну радиологију након ревидиране ФИГО стадијума 2018. Еур. Радиол. 2021, 31, 7802–7816. [ЦроссРеф]
18. Лин, И.; Цхен, З.; Куанг, Ф.; Ли, Х.; Зхонг, К.; Ма, М. Евалуација карцинома грлића материце стадијума ИБ међународне федерације гинекологије и акушерства: Поређење дифузионо пондерисане и динамичке магнетне резонанције са појачаним контрастом на 3.0 ТЈ Цомпут. Асист. Томогр. 2013, 37, 989–994. [ЦроссРеф]
19. Парк, ЈЈ; Ким, ЦК; Парк, СИ; Парк, БК Параметријална инвазија код рака грлића материце: фузионисана Т2-пондерисана слика и дифузно-пондерисана слика високе б-вредности са потискивањем позадинског сигнала тела на 3 Т. Радиологи 2015, 274, 734–741. [ЦроссРеф]
20. Парк, КЈ; Браски-Амирфарзан, М.; ДиПиро, ПЈ; Гиардино, АА; Јаганнатхан, ЈП; Ховард, СА; Схинагаре, АБ; Крајевски, КМ Мултимодално снимање локално рекурентног и метастатског карцинома грлића материце: нагласак на хистологији, прогнози и управљању. Абдом. Радиол. 2016, 41, 2496–2508. [ЦроссРеф] [ПубМед]
21. Сала, Е.; Роцкалл, А.; Рангарајан, Д.; Кубик-Хуцх, РА Улога магнетне резонанце са динамичким контрастом и дифузијом у женској карлици. ЕУР. Ј. Радиол. 2010, 76, 367–385. [ЦроссРеф]
22. Лиу, И.; Баи, Р.; Сун, Х.; Лиу, Х.; Зхао, Кс. Диффусион-веигхтед имагинг у предвиђању и праћењу одговора рака грлића материце на комбиновану хеморадијацију. Цлин. Радиол. 2009, 64, 1067–1074. [ЦроссРеф] [ПубМед]
23. Харри, ВН Нове технике снимања као биомаркери одговора код рака грлића материце. Гинецол. Онцол. 2010, 116, 253–261. [ЦроссРеф] [ПубМед]
24. Аказава, М.; Хасхимото, К. Вештачка интелигенција код гинеколошких карцинома: тренутни статус и будући изазови—систематски преглед. Артиф. Интелл. Мед. 2021, 120, 102164. [ЦроссРеф] [ПубМед]
25. Бокхман, ЈВ Два патогенетска типа карцинома ендометријума. Гинецол. Онцол. 1983, 15, 10–17. [ЦроссРеф]
26. Бедди, П.; Моиле, П.; Катаока, М.; Иамамото, АК; Јоуберт, И.; Ломас, Д.; Цравфорд, Р.; Сала, Е. Евалуација дубине инвазије миометријума и укупног стадијума у карциному ендометријума: поређење дифузионо-пондерисаног и динамичког МР сликања са побољшаним контрастом. Радиологија 2012, 262, 530–537. [ЦроссРеф]
27. Рецхицхи, Г.; Галимберти, С.; Сигнорелли, М.; Перего, П.; Валсеццхи, МГ; Сирони, С. Инвазија миометријума код рака ендометријума: Дијагностичке перформансе дифузионо пондерисаног МР снимања на 1.5-Т. ЕУР. Радиол. 2009, 20, 754–762. [ЦроссРеф]
28. Родригез-Ортега, А.; Алегре, А.; Лаго, В.; Царот-Сиерра, ЈМ; Бме, АТ; Монтолиу, Г.; Доминго, С.; Алберицх-Баиарри, А.; Марти-Бонмати, Л. Интеграција прогностичких биомаркера магнетне резонанце заснована на машинском учењу за стратификацију инвазије миометрија код рака ендометријума. Ј. Магн. Ресон. Имагинг 2021, 54, 987–995. [ЦроссРеф]
29. Лакхман, И.; Веерарагхаван, Х.; Цхаим, Ј.; Феиер, Д.; Голдман, ДА; Московитз, ЦС; Ноугарет, С.; Соса, РЕ; Варгас, ХА; Сослов, РА; ет ал. Диференцијација леиомиосаркома материце од атипичног леиомиома: дијагностичка тачност квалитативних карактеристика МР снимања и изводљивост анализе текстуре. ЕУР. Радиол. 2017, 27, 2903–2915. [ЦроссРеф]
30. Вираркар, М.; Диаб, Р.; Палмкуист, С.; Бассетт, ЈР; Бхосале, П. Дијагностичка изведба МРИ за разликовање лејомиосаркома материце од бенигног лејомиома: мета-анализа. Ј. Белг. Соц. Радиол. 2020, 104, 69. [ЦроссРеф]
31. Вахаб, ЦА; Јаннот, А.-С.; Бонаффини, ПА; Боуриллон, Ц.; Цорноу, Ц.; Лефрере-Белда, М.-А.; Батс, А.-С.; Тхомассин-Наггара, И.; Беллуцци, А.; Реинхолд, Ц.; ет ал. Дијагностички алгоритам за разликовање бенигних атипичних леиомиома од малигних саркома материце помоћу дифузионо-пондерисане МРИ. Радиологија 2020, 297, 361–371. [ЦроссРеф]
32. Фујии, С.; Каките, С.; Нишихара, К.; Кавасаки, И.; Харада, Т.; Кигава, Ј.; Каминоу, Т.; Огава, Т. Дијагностичка прецизност дифузионо-пондерисане слике у разликовању бенигних од малигних лезија јајника. Ј. Магн. Ресон. Имагинг 2008, 28, 1149–1156. [ЦроссРеф] [ПубМед]
33. Форстнер, Р.; Тхомассин-Наггара, И.; Цунха, ТМ; Кинкел, К.; Масселли, Г.; Кубик-Хуцх, Р.; Спенцер, ЈА; Роцкалл, А. ЕСУР препоруке за МР снимање сонографски неодређене аднексалне масе: ажурирање. ЕУР. Радиол. 2017, 27, 2248–2257. [ЦроссРеф] [ПубМед]
34. Тхомассин-Наггара, И. Допринос дифузионо пондерисане МР слике за предвиђање бенигности сложених аднексалних маса. ЕУР. Радиол. 2009, 19, 1544–1552. [ЦроссРеф] [ПубМед]
35. Данда, С.; Тхакур, М.; Керкар, Р.; Јагмохан, П. Диффусион-веигхтед Имагинг оф Гинецологиц Туморс: Диагностиц Пеарлс анд Потентиал Питфаллс. Радиографија 2014, 34, 1393–1416. [ЦроссРеф]
36. Тхомассин-Наггара, И.; Понцелет, Е.; Јалагуиер-Цоудраи, А.; Гуерра, А.; Фоурниер, ЛС; Стојановић, С.; Миллет, И.; Бхарвани, Н.; Јухан, В.; Цунха, ТМ; ет ал. Систем података за извештавање о јајницима и аднексима Магнетна резонанца (О-РАДС МРИ) Оцена за стратификацију ризика ултразвучно неодређених аднексалних маса. ЈАМА Нетв. Отворено 2020, 3, е1919896. [ЦроссРеф] [ПубМед]
37. Садовски, ЕА; Тхомассин-Наггара, И.; Роцкалл, А.; Матурен, КЕ; Форстнер, Р.; Јха, П.; Ноугарет, С.; Сиегелман, ЕС; Реинхолд, Ц. О-РАДС МРИ систем стратификације ризика: Водич за процену лезија аднекса од АЦР О-РАДС комитета. Радиологи 2022, 303, 204371. [ЦроссРеф]
38. Аслан, С.; Тосун, СА Дијагностичка тачност и валидност резултата О-РАДС МРИ на основу поједностављеног МРИ протокола: Ретроспективна студија једног терцијарног центра. Ацта Радиол. 2021. [ЦроссРеф]
39. Вонг, ВК; Кундра, В. Перформансе О-РАДС МРИ резултата за класификацију неодређених аднексалних маса у САД. Радиол. Имагинг Цанцер 2021, 3, е219008. [ЦроссРеф]
40. Левине, Д. МРИ О-РАДС: Учење о новом систему стратификације ризика. Радиологи 2022, 303, 211307. [ЦроссРеф]
41. Фоурниер, ЛС; Боуриллон, Ц.; Бриса, М.; Роуссеау, Ц. ИРМ де диффусион данс ле пелвис феминин: Принципес, техника, пиегес ет артефацтс. Имаг. Фемме 2015, 25, 8–15. [ЦроссРеф]
42. Ноугарет, С.; Тирумани, СХ; Аддлеи, Х.; Пандеи, Х.; Сала, Е.; Реинхолд, Ц. Бисери и замке у МРИ гинеколошког малигнитета са дифузионо-пондерисаном техником. Сам. Ј. Роентгенол. 2013, 200, 261–276. [ЦроссРеф] [ПубМед]
Тхомас Де Перрот 1, Цхристине Садјо Зоуа 1 , Царл Г. Глессген 1 , Диомидис Ботсикас 1 , Лена Берцхтолд 2 , Рарес Саломир 1 , Сопхие Де Сеигнеук 2 , Харриет Ц. Тхоени 3 и Јеан-Паул Валлее 1
1 Одсек за радиологију, Универзитетске болнице у Женеви и Универзитет у Женеви, 1205 Женева, Швајцарска; christine.sadjo@hcuge.ch (ЦСЗ); carl.glessgen@hcuge.ch (ЦГГ); diomidis.botsikas@hcuge.ch (ДБ); raresvincent.salomir@hcuge.ch (РС); јеан-paul.vallee@hcuge.ch (Ј.-ПВ)
2 Одсек за нефрологију, Универзитетске болнице у Женеви, 1205 Женева, Швајцарска; lena.berchtold@hcuge.ch (ЛБ); sophie.deseigneux@hcuge.ch (СДС)
3 Дивисион оф Радиологи, Хопитал Цантонал Фрибоургоис, 1752 Вилларс-сур-Глане, Швајцарска; харриет.тхоени@х-фр.цх






